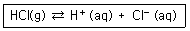스터디모드 10문제
진행중
문제를 풀지않고 휴식하면서 학습할 수 있는 모드입니다.
278155
2903
1. 다음 반응에서 ΔH° = -75.2kJ/mol, ΔS° = -132J/K·mol 일 때의 설명으로 옳은 것은?(단, ΔH° 와 ΔS° 각각 표준엔탈피 변화와 표준엔트로피 변화를 의미하며 온도에 관계없이 일정하다고 가정한다.
[1]
오류 내용 신고
2903
https://gongquiz.com/main/pages/search.php?q=%ED%99%94%ED%95%99%EB%B6%84%EC%84%9D%EA%B8%B0%EC%82%AC%28%EA%B5%AC%29
https://gongquiz.com/main/pages/%EB%8B%A4%EC%9D%8C+%EB%B0%98%EC%9D%91%EC%97%90%EC%84%9C+%CE%94H%C2%B0+%3D+-75+2kJ%2Fmol%2C+%CE%94S%C2%B0+%3D+-132J%2FK%C2%B7mol+%EC%9D%BC+%EB%95%8C%EC%9D%98+.quiz??mode=study&quizNo=278155&historyNo=reset
[]
[278155,278156,278157,278158,278159,278160,278161,278163,278164,278165]
{"278155":[1,2,3,4],"278156":[1,2,3,4],"278157":[1,2,3,4],"278158":[1,2,3,4],"278159":[1,2,3,4],"278160":[1,2,3,4],"278161":[1,2,3,4],"278163":[1,2,3,4],"278164":[1,2,3,4],"278165":[1,2,3,4]}
study
123130778
-1
0
0
다음 반응에서 ΔH° = -75.2kJ/mol, ΔS° = -132J/K·mol 일 때의... - 화학분석기사(구) (2017년 9월 23일 기출문제) #공퀴즈 #닷컴

 페이스북
페이스북 트위터
트위터 네이버
네이버 네이버블로그
네이버블로그 카카오톡
카카오톡 라인
라인 밴드
밴드 카카오스토리
카카오스토리 URL 복사
URL 복사